Witaj w fascynującym świecie osmozy zjawiska, które choć niewidoczne, odgrywa kluczową rolę w każdym aspekcie życia, od funkcjonowania naszych komórek po procesy zachodzące w kuchni. Ten artykuł rozwieje wszelkie wątpliwości dotyczące tego fundamentalnego mechanizmu, wyjaśniając jego definicję, działanie, znaczenie dla organizmów żywych oraz praktyczne zastosowania, w tym rewolucyjną technologię odwróconej osmozy.
Osmoza: klucz do zrozumienia ruchu wody i równowagi w przyrodzie
- Osmoza to spontaniczne przenikanie rozpuszczalnika (najczęściej wody) przez błonę półprzepuszczalną.
- Kluczowe elementy to błona półprzepuszczalna (przepuszcza wodę, zatrzymuje substancje rozpuszczone) i różnica stężeń.
- Jest to specyficzny rodzaj dyfuzji, różniący się od niej koniecznością obecności błony i selektywnością transportu.
- Ma fundamentalne znaczenie dla życia, regulując gospodarkę wodną w komórkach roślinnych (turgor) i zwierzęcych.
- Znajduje zastosowanie w życiu codziennym (konserwacja żywności) i technologii (filtry do wody, odsalanie).
- Odwrócona osmoza to wymuszony przepływ wody pod ciśnieniem, wykorzystywany do oczyszczania i odsalania.
Czym tak naprawdę jest osmoza? Prosta definicja zjawiska, które dotyczy każdego z nas
Osmoza w kilku słowach: ruch wody w poszukiwaniu równowagi
Osmoza to proces fizykochemiczny, który polega na samorzutnym przenikaniu rozpuszczalnika, najczęściej wody, przez specjalną barierę zwaną błoną półprzepuszczalną. Wyobraź sobie, że woda przemieszcza się sama, podążając od miejsca, gdzie jest jej "więcej" (czyli tam, gdzie jest mniej rozpuszczonych substancji), do miejsca, gdzie jest jej "mniej" (czyli tam, gdzie jest więcej rozpuszczonych substancji). Głównym celem tego ruchu jest wyrównanie stężeń po obu stronach tej błony. To fundamentalne zjawisko, które wpływa na wiele procesów w naturze i naszym otoczeniu.
Kluczowi gracze w procesie: błona półprzepuszczalna i różnica stężeń
Aby osmoza mogła zajść, potrzebujemy dwóch kluczowych elementów. Pierwszym jest błona półprzepuszczalna. Możemy ją sobie wyobrazić jako sito o bardzo drobnych oczkach przepuszcza ono małe cząsteczki wody, ale zatrzymuje większe cząsteczki rozpuszczonych substancji, takich jak sole czy cukry. Drugim kluczowym graczem jest różnica stężeń, czyli nierównomierne rozmieszczenie substancji rozpuszczonych po obu stronach błony. Ta różnica stężeń działa jak siła napędowa, która "popycha" wodę w stronę obszaru o wyższym stężeniu, dążąc do jego zmniejszenia.
Dlaczego osmoza to nie to samo co dyfuzja? Najważniejsze różnice, które warto znać
Często słyszymy o osmozie w kontekście dyfuzji i łatwo je pomylić. Dyfuzja to ogólne zjawisko samorzutnego ruchu cząsteczek z obszaru o wyższym stężeniu do obszaru o niższym stężeniu, mające na celu wyrównanie tej różnicy. Dyfuzja może zachodzić w gazach, cieczach, a nawet ciałach stałych, i nie wymaga obecności żadnej błony. Osmoza jest natomiast specyficznym rodzajem dyfuzji. Dotyczy ona wyłącznie przenikania rozpuszczalnika (najczęściej wody) przez błonę półprzepuszczalną. Czyli, mówiąc obrazowo, dyfuzja to ogólny ruch wszystkiego w celu wyrównania, a osmoza to ruch tylko wody przez specjalną "siatkę" w celu wyrównania stężeń.
Jak działa osmoza? Mechanizm krok po kroku
Czym są roztwory hipotoniczne, hipertoniczne i izotoniczne?
Aby w pełni zrozumieć mechanizm osmozy, musimy poznać trzy kluczowe pojęcia dotyczące stężeń roztworów w porównaniu do wnętrza komórki. Roztwór hipotoniczny to taki, który ma niższe stężenie substancji rozpuszczonych niż wnętrze komórki. Gdy komórka znajdzie się w takim środowisku, woda będzie do niej napływać, powodując jej pęcznienie. Z kolei roztwór hipertoniczny ma wyższe stężenie substancji rozpuszczonych niż w komórce. W tym przypadku woda będzie opuszczać komórkę, prowadząc do jej kurczenia się. Wreszcie, roztwór izotoniczny ma takie samo stężenie substancji rozpuszczonych jak w komórce. W takim środowisku woda przepływa przez błonę w obu kierunkach z taką samą prędkością, więc komórka nie zmienia swojej objętości ani kształtu. Wyobraźmy sobie to na przykładzie: jeśli zanurzymy rodzynkę (komórkę roślinną) w czystej wodzie (roztwór hipotoniczny), napęcznieje. Jeśli zanurzymy ją w bardzo słodkim syropie (roztwór hipertoniczny), skurczy się.Ciśnienie osmotyczne: niewidzialna siła napędzająca cały proces
Ciśnienie osmotyczne to siła, która "ciągnie" wodę do roztworu o wyższym stężeniu substancji rozpuszczonej przez błonę półprzepuszczalną. Jest to miara tendencji roztworu do pobierania wody przez osmozę. Im wyższe stężenie substancji rozpuszczonej, tym wyższe ciśnienie osmotyczne i tym silniejszy jest "pociąg" wody. To właśnie ta niewidzialna siła napędza cały proces osmozy, dążąc do wyrównania stężeń po obu stronach błony.
Co się dzieje, gdy stężenia po obu stronach błony się wyrównają?
Gdy stężenia substancji rozpuszczonej po obu stronach błony półprzepuszczalnej się wyrównają, osiągamy stan nazywany równowagą osmotyczną. W tym momencie ruch netto wody ustaje. Oznacza to, że cząsteczki wody nadal przemieszczają się przez błonę, ale ich przepływ w jednym kierunku jest równoważony przez przepływ w kierunku przeciwnym. Zjawisko to prowadzi do stabilizacji stężeń i ustabilizowania się sytuacji po obu stronach błony. Komórka w roztworze izotonicznym znajduje się właśnie w takim stanie równowagi.
Dlaczego bez osmozy nie byłoby życia? Kluczowa rola w świecie przyrody
Osmoza w komórkach roślinnych: sekret jędrności i wzrostu
Osmoza jest absolutnie kluczowa dla życia roślin. To dzięki niej rośliny są w stanie pobierać wodę z gleby przez korzenie. Woda, która jest mniej stężona niż płyny w komórkach korzeniowych, przenika do nich właśnie na drodze osmozy. Następnie, dzięki procesom osmotycznym zachodzącym w kolejnych komórkach, woda przemieszcza się w górę rośliny, docierając do liści i kwiatów. Bez tego mechanizmu rośliny nie mogłyby funkcjonować, rosnąć ani utrzymywać swojej struktury.
Co to jest turgor i dlaczego zwiędnięta roślina po podlaniu odzyskuje siły?
Turgor to nic innego jak ciśnienie wywierane przez wodę znajdującą się wewnątrz komórki roślinnej na jej ścianę komórkową. Kiedy komórka roślinna jest dobrze nawodniona (dzięki osmozie), ściana komórkowa jest napięta, co nadaje roślinie jędrność i sztywność. To właśnie dlatego zwiędnięta roślina, która straciła wodę i której komórki stały się wiotkie, po podlaniu odzyskuje swoje siły. Woda napływa do komórek na drodze osmozy, zwiększając ciśnienie turgorowe i przywracając roślinie witalność.Plazmoliza, czyli co się dzieje z rośliną w zbyt słonej glebie
Zjawisko plazmolizy to niestety ciemna strona osmozy dla roślin. Zachodzi ono, gdy roślina znajdzie się w środowisku o bardzo wysokim stężeniu substancji rozpuszczonych, na przykład w nadmiernie zasolonej glebie. W takiej sytuacji woda zaczyna opuszczać komórki roślinne na drodze osmozy, próbując wyrównać stężenie z otoczeniem. Prowadzi to do kurczenia się protoplastu (zawartości komórki) i jego odrywania się od ściany komórkowej. Plazmoliza jest dla rośliny bardzo szkodliwa i może prowadzić do jej obumarcia.Osmoza w komórkach zwierzęcych: strażnik równowagi wewnętrznej
Również w organizmach zwierzęcych, w tym w naszym ciele, osmoza odgrywa nieocenioną rolę. Jest ona kluczowa dla utrzymania homeostazy czyli stabilnej równowagi środowiska wewnętrznego. Komórki zwierzęce, pozbawione sztywnych ścian komórkowych jak rośliny, są bardziej wrażliwe na zmiany stężenia płynów. Osmoza reguluje przepływ wody między komórkami a otaczającymi je płynami ustrojowymi, zapewniając prawidłowe funkcjonowanie wszystkich tkanek i narządów.
Jak osmoza wpływa na ludzkie komórki krwi?
Nasze czerwone krwinki, czyli erytrocyty, są doskonałym przykładem tego, jak osmoza wpływa na komórki zwierzęce. Jeśli umieścimy je w roztworze hipotonicznym (np. czystej wodzie), zaczną one pęcznieć i mogą nawet eksplodować, ponieważ woda napływa do nich zbyt szybko. W roztworze hipertonicznym (np. bardzo słonej wodzie) erytrocyty skurczą się, tracąc wodę. Dopiero w roztworze izotonicznym, o odpowiednim stężeniu soli, erytrocyty zachowują swój prawidłowy kształt i funkcję. To pokazuje, jak ważne jest utrzymanie właściwego stężenia płynów w naszym organizmie.
Gospodarka wodno-elektrolitowa a znaczenie prawidłowego nawodnienia
Wszystkie te procesy osmotyczne składają się na złożoną gospodarkę wodno-elektrolitową organizmu. Prawidłowe nawodnienie jest niezbędne do tego, aby nasze komórki mogły efektywnie wymieniać substancje z otoczeniem i wykonywać swoje funkcje. Osmoza jest kluczowym mechanizmem, który pomaga utrzymać właściwy bilans wody i elektrolitów w organizmie, zapewniając jego prawidłowe funkcjonowanie. Dlatego tak ważne jest picie odpowiedniej ilości płynów każdego dnia.
Osmoza na co dzień: gdzie możesz zaobserwować to zjawisko?
Twoja kuchnia jako laboratorium: solenie warzyw i marynowanie mięsa
Osmoza jest obecna w naszej kuchni na co dzień, często nawet o tym nie wiemy! Kiedy solimy warzywa, na przykład ogórki do sałatki, wysokie stężenie soli na powierzchni warzywa powoduje wyciąganie z nich wody na drodze osmozy. Podobnie dzieje się podczas marynowania mięsa płyny, które zawierają przyprawy i inne składniki marynaty, mogą wnikać w strukturę mięsa, wpływając na jego smak i teksturę. To wszystko dzięki ruchowi wody napędzanemu różnicą stężeń.
Dlaczego palce marszczą się w wodzie? Zaskakująca rola osmozy
Czy zastanawialiście się kiedyś, dlaczego po długiej kąpieli nasze palce u rąk i nóg zaczynają się marszczyć? Jedno z najpopularniejszych wyjaśnień tego zjawiska wiąże się właśnie z osmozą. Woda, która ma niższe stężenie substancji rozpuszczonych niż nasze komórki skóry, przenika do nich na drodze osmozy. Powoduje to pęcznienie komórek i zwiększenie objętości naskórka, co w połączeniu z jego elastycznością prowadzi do charakterystycznego marszczenia. Choć istnieją też inne teorie, osmoza jest tu z pewnością ważnym czynnikiem.
Konserwacja żywności: jak osmoza pomaga zachować trwałość produktów?
Osmoza jest od wieków wykorzystywana do konserwowania żywności. Procesy takie jak solenie ryb czy przygotowywanie dżemów i konfitur opierają się na tym zjawisku. Dodanie dużej ilości soli lub cukru tworzy środowisko hipertoniczne wokół produktu. Wysokie stężenie soli lub cukru na zewnątrz komórek drobnoustrojów (bakterii, pleśni) powoduje, że woda opuszcza te komórki na drodze osmozy. Odwodnione drobnoustroje nie mogą się rozwijać, co znacząco przedłuża trwałość żywności. To prosty, ale niezwykle skuteczny sposób na zachowanie jej świeżości.
Odwrócona osmoza – kiedy proces biegnie w drugą stronę?
Na czym polega fenomen odwróconej osmozy?
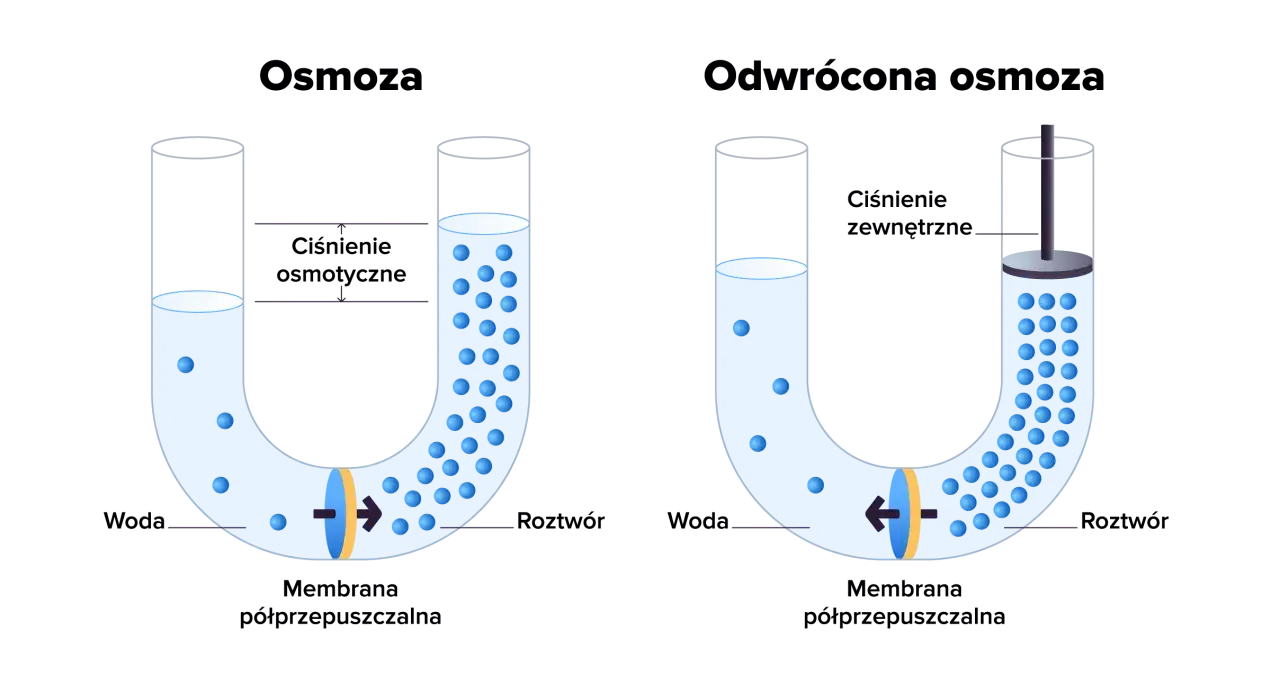
Odwrócona osmoza to fascynujący proces, który działa w przeciwnym kierunku do naturalnej osmozy. W tym przypadku nie pozwalamy wodzie samorzutnie przenikać z niższego do wyższego stężenia. Zamiast tego, przy użyciu zewnętrznego ciśnienia, które jest wyższe niż naturalne ciśnienie osmotyczne, wymuszamy przepływ rozpuszczalnika (wody) z roztworu o wyższym stężeniu do roztworu o niższym stężeniu. Dzieje się to zazwyczaj przy użyciu specjalnych membran, które zatrzymują substancje rozpuszczone, pozwalając przejść tylko czystej wodzie. To technologia, która zrewolucjonizowała wiele dziedzin.
Filtry do wody w Twoim domu: jak technologia odwróconej osmozy zapewnia krystaliczną czystość?
Jednym z najbardziej znanych zastosowań odwróconej osmozy są domowe systemy filtracji wody. Filtry RO (Reverse Osmosis) wykorzystują półprzepuszczalne membrany, które pod wpływem ciśnienia sieci wodociągowej skutecznie usuwają z wody niemal wszystkie zanieczyszczenia. Są to między innymi metale ciężkie, sole mineralne, chlor, bakterie, wirusy, a nawet pestycydy. W efekcie otrzymujemy wodę o wyjątkowej czystości, idealną do picia i gotowania. Według danych Superprof, systemy te są coraz popularniejsze ze względu na skuteczność i jakość uzyskanej wody.
Przeczytaj również: Jak zdać maturę z biologii: sprawdzone metody na sukces i pewność siebie
Od odsalania wody morskiej po zastosowania w przemyśle: potęga odwróconej osmozy
Zastosowania odwróconej osmozy wykraczają daleko poza nasze domy. Jest to kluczowa technologia w procesie odsalania wody morskiej, co ma ogromne znaczenie dla regionów z deficytem wody pitnej. Ogromne instalacje odsalające wykorzystują odwróconą osmozę do przekształcania słonej wody w wodę zdatną do spożycia. Ponadto, technologia ta znajduje szerokie zastosowanie w przemyśle spożywczym (np. do produkcji soków, mleka), farmaceutycznym (produkcja leków i płynów infuzyjnych), a nawet w przemyśle elektronicznym do produkcji ultra czystej wody.